
오늘(14일) 대한화장품협회가 마련한 ‘미국 화장품 규제 현대화법(MoCRA) 웨비나’는 최대 접속인원 289명에 40여 개 질문이 쏟아질 정도로 열기가 뜨거웠다.
강의를 맡은 엠톰글로벌(MTOM Global) 존 권(John Kwon) 대표는 ‘OMUFA 수수료 프로그램’으로 이미 익숙한 얼굴. 실시간 질문에 성심껏 답하고 추후 업데이트를 통해 북미시장의 화장품·의료기기 관련 ‘친절한 컨설턴트’로 널리 알려져 있다.
미국은 2022년 12월 29일 ‘화장품 규제 현대화법(MoCRA : Modernization of Cosmetics Regulation Act of 2022)'이 포함된 ‘2023년 통합 세출법’을 통과시켰다. 이 법은 연방 식품, 의약품 및 화장품법(FDCA)의 Ⅵ장에 새로운 사항을 추가해 준수를 요구한다. MoCRA가 생긴 배경은 미국 의회의 소비자 보호 의견과 지난 1938년 이후 85년 만의 변화를 담은 새로운 규제 신설 요구다.
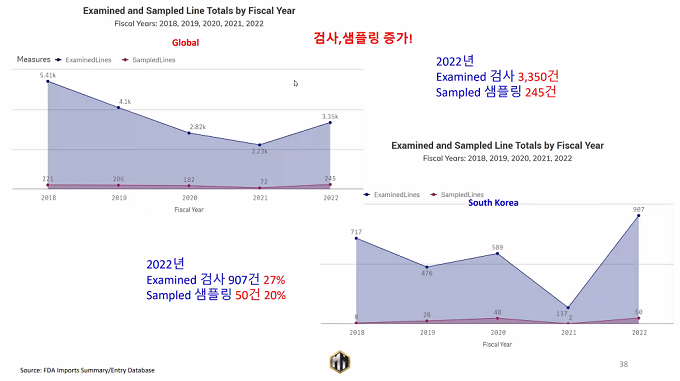
우리로서는 유럽·중국의 규제에 상응하는 미국의 조치로 이해된다. 또한 한국 화장품의 위상 변화다. 미국 화장품시장에서 한국산 화장품 물량은 228만톤(수입물량의 12%)에 달한다.(’22년, 캐나다, 중국에 이어 3위 랭크) 이렇다 보니 △화장품 검사 건수 3350건 중 한국산 907건(27%) △샘플링 245건 중 한국산 50건(20%) 등을 차지할 정도로 민감해졌다.
최근 5년 동안 수입거부도 전체 3661건 중 한국이 480건이나 됐다. 2022년만 해도 전체 수입 거부 1050건 중 118건으로 전체 거부건수의 11%나 된다. 한국 화장품기업들이 MoCRA 시행에 긴장하는 배경이다.
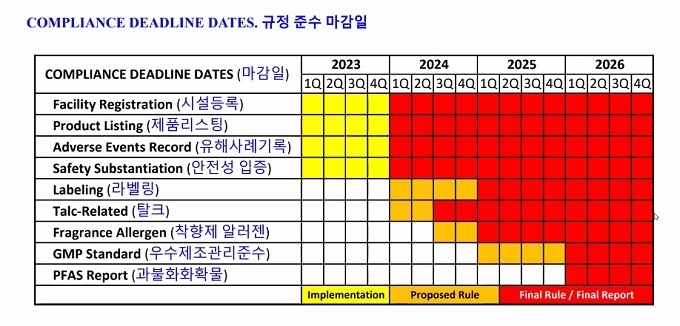
먼저 MoCRA 시행 일정을 보면 △시설등록(facility registration) △제품 리스팅(product listing) △유해사례 기록(adverse events record) △안전성 입증(safety substantiation) 등은 오는 2023년 12월 29일까지 등록해야 한다. 신규 제조업체라면 첫 제조 활동 후 60일 안에 등록해야 한다.
이어 △라벨링(labelling)은 2024년 4Q △탈크(talc-related) 2024년 2Q △착향제 알러젠 2024년 4Q △GMP 기준 2025년 4Q △과불화화합물 2025년 4Q 등으로 예정돼 있다.
존권 대표는 “앞의 4가지는 올해 말까지 등록해야 하며, 나머지는 가이드 마련이 된 후에야 상세한 일정을 알 수 있다”고 전했다.
질문 내용은 ▲시설 등록 ▲제품 리스팅 등록 ▲책임자 등록 ▲제품 라벨링 등에 많이 쏠렸다.
제조사 등록은 필수이며 만일 미등록시 미국 내 제조·수출입·유통 모두 할 수 없다. 책임자로는 제조사, 포장업자, 유통업체 중 누구나 등록 가능하다. 시설등록비용에 대해 존권 대표는 “화장품의 경우 2년마다 갱신을 해야 한다고 나와 있어 2년마다 내야 할 것으로 예측하고 있다. 현재 FDA에서 MoCRA 관련 가이드라인, 비용, 시스템 구축 등 공식 발표 되면 업데이트 해드리겠다”고 말했다.
만약 FDA로부터 문제점(Warning Letter, OTC inspection fail, Import Alert)을 지적받은 경우에는 재검사 또는 시정조치를 해결한 후 등록해야 한다. 또 OTC제조와 달리 화장품 제조의 GMP 기준은 ISO 22716을 준수(미국 협회)하는 선에서 결정이 될 가능성이 있다고 존권 대표는 설명했다.
화장품 자발적 등록 프로그램(VCRP)은 대체될 예정이다. 존권 대표는 “기존 VCRP의 업그레이드가 시간과 비용 측면에서 효율적이므로 그 방법을 선택할 것으로 보인다. 새로운 MoCRA에서도 제품 리스팅 등록은 의무적으로 해야 한다”고 전했다.
화장품 용기나 단상자에는 미국 내 주소, 미국 내 전화번호, 이메일 같은 전자 연락처 등 세 가지 모두 기재된 라벨이 부착되어야 한다. 존권 대표는 “책임자가 해당 화장품의 부작용 보고를 받을 수 있어야 한다. 이메일, 웹사이트 등이 포함된다”고 강조했다.
이밖에 소규모기업은 최근 3년 평균 연 매출이 100만달러 이하여야 해당된다. FDA가 모니터링 하므로 변동 시 지체없이 신고하는 게 좋다고 존권 대표는 조언했다. 동물실험도 의회의 폐지 요구에 따라 별도 가이드라인이 마련될 예정이다.
존권 대표는 “FDA가 유럽 CPNP나 중국 NMPA 등을 벤치마킹하고 있다. 지난 85년간 업데이트 되지 않았던 화장품 규제 중 어떤 내용이 포함될지 많은 화장품기업과 단체들의 관심이 크다”고 분위기를 전했다.
한편 대한화장품협회 김경옥 부장은 “웨비나 내용 및 질의사항을 정리해 홈페이지에 영상 및 관련 내용을 업데이트 할 예정”이라고 밝혔다.































